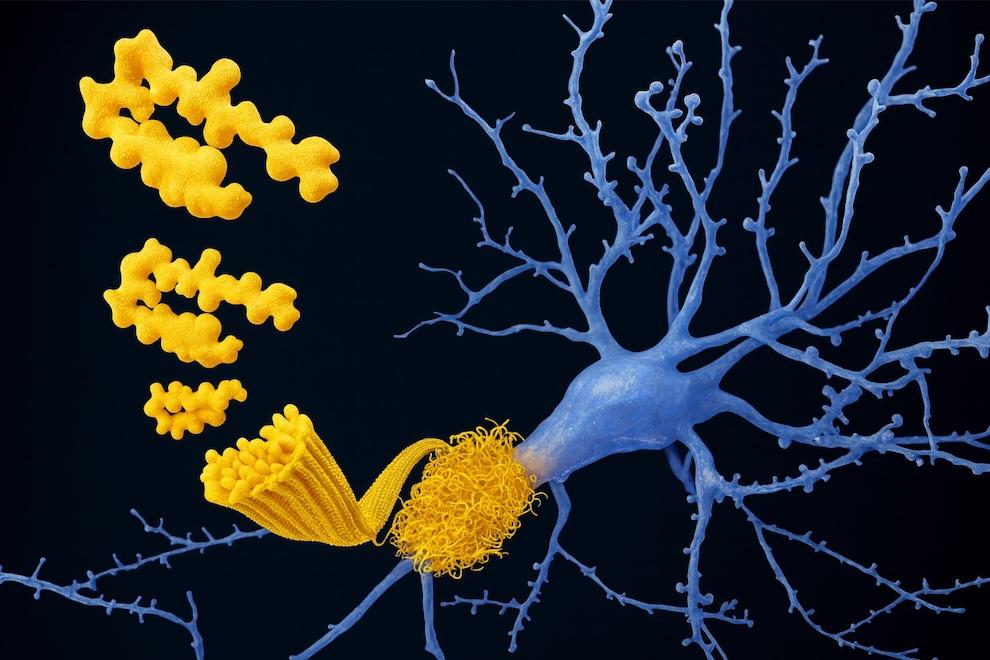
Si cuidas de una persona con alzhéimer, seguramente has oído hablar de la proteína beta amiloide.
Aunque pueda sonarte lejana, lo cierto es que entender qué papel juega en la enfermedad también te ayudará a comprender mejor lo que le ocurre a tu ser querido.
En este artículo, vamos a explicarte de forma sencilla qué es exactamente la beta amiloide, qué funciones tiene en un cerebro sano, y por qué su desequilibrio está en el centro del desarrollo del alzhéimer.
Verás cómo se produce, cómo afecta a las neuronas cuando se acumula y qué avances científicos nos están acercando a nuevos tratamientos.
También te aconsejaremos sobre los hábitos saludables que pueden ayudarte a proteger la salud cerebral de la persona que cuidas (y también la tuya).
¿Qué es la proteína beta amiloide?
La beta amiloide es una pequeña cadena de aminoácidos (entre 36 y 43 unidades) que el cerebro produce de manera completamente natural todos los días.
En realidad, es un fragmento diminuto que se origina cuando una molécula mucho más grande, llamada proteína precursora amiloidea (APP), se divide en partes más pequeñas.
Esta, la APP, es una proteína que encontramos en muchas partes de nuestro cuerpo, pero especialmente en las conexiones entre neuronas (las células que forman nuestro cerebro).
Cuando esta proteína se «rompe» o procesa de forma natural, uno de los fragmentos que se genera es la beta amiloide, otra proteína.
La beta amiloide participa en el funcionamiento normal del cerebro y, de hecho, tiene funciones protectoras.
Sin embargo, para que esto sea así debe cumplirse el proceso natural mediante el que tal y como se genera, se elimina cuando ya no se necesita.
El motivo es que cuando comienza a acumularse, forma estructuras dañinas que interfieren con la comunicación entre neuronas. Esto es precisamente lo que ocurre en el alzhéimer.
Por lo tanto, el problema no es la presencia de beta amiloide, sino la descompensación del sistema de producción y eliminación.
Función normal de la beta amiloide en el cerebro
En condiciones normales, la beta amiloide actúa como un verdadero «guardián cerebral» que protege y mantiene la salud de las neuronas. Entre sus funciones, están:
- Proteger a las neuronas del estrés oxidativo originado por los radicales libres.
- Participar en el metabolismo del colesterol, contribuyendo a regular sus niveles.
- Defender al cerebro de microorganismos patógenos (bacterias, hongos o virus) mediante estructuras que los atrapan y eliminan.
- Activar las enzimas responsables de la transmisión de señales dentro de las células nerviosas.
- Proveer la glucosa que las neuronas necesitan para funcionar.
En definitiva: cuando la beta amiloide funciona correctamente, mantiene las neuronas protegidas del daño, asegura que tengan la energía necesaria para funcionar, y facilita la comunicación entre ellas.
Producción y metabolismo de la proteína beta amiloide
Para entender cómo se produce la beta amiloide, primero necesitas conocer a los actores principales de este proceso:
- La APP (proteína precursora amiloidea) es como una molécula madre que debe ser «cortada» por enzimas especializadas.
- Las secretasas son las «tijeras moleculares» que realizan estos cortes. Existen tres tipos principales: α-secretasa, β-secretasa y γ-secretasa.
Ahora sí, el proceso de formación de beta amiloide puede seguir dos caminos diferentes:
- Vía saludable (no amiloidogénica): la α-secretasa corta la APP y este corte impide que se forme beta amiloide. Los fragmentos resultantes son solubles y fáciles de eliminar, por lo que no se produce acumulación patológica de beta amiloide. Esta es la vía predominante en cerebros sanos.
- Vía problemática (amiloidogénica): primero actúa la β-secretasa, que hace el primer corte en la APP. Luego interviene la γ-secretasa, que realiza el segundo corte. Este proceso produce diferentes tipos de beta amiloide: Aβ1-40 (40 aminoácidos) y Aβ1-42 (42 aminoácidos). La primera es más soluble y menos propensa a formar agregados tóxicos, al contrario que la segunda, que es la que está más relacionada con el desarrollo de alzhéimer.
Un cerebro sano produce ambas formas de beta amiloide (principalmente Aβ1-40), pero predomina la vía no amiloidogénica que impide la acumulación patológica.
Una vez sabido esto, la pregunta es: ¿qué hace que se active una vía u otra?
El equilibrio entre estas vías depende de factores como la edad, la genética, el estrés, la inflamación y el estilo de vida.
Con el envejecimiento o en presencia de factores de riesgo, puede activarse más la vía problemática.
Beta amiloide y alzhéimer: ¿qué relación existe?
La relación entre la beta amiloide y el alzhéimer ha dado lugar a una teoría científica conocida como la «hipótesis de la cascada amiloide».
Esta teoría, formulada en 1992, propone que la acumulación anormal de beta amiloide en el cerebro es el evento inicial que desencadena toda una cascada de procesos dañinos que llevan al alzhéimer.
Esta hipótesis es la que ha proporcionado respuestas en cuanto al rol de esta proteína y cómo afecta a las neuronas.
Rol de la beta amiloide en el desarrollo del alzhéimer
Según la mencionada teoría, cuando el sistema de producción de la beta amiloide se desregula, los mecanismos de eliminación de la beta amiloide fallan y se almacenan los desechos.
En paralelo, aumenta la producción de la forma de beta amiloide que tiende a formar agregados, la Aβ1-42.
Esta sobreproducción es el primer eslabón de la cadena que conduce al desarrollo del alzhéimer, pues se crea el ambiente propicio para la formación de placas y el daño neuronal característico de la patología.
Cómo afectan las placas beta amiloides a las neuronas
Cuando la beta amiloide se acumula en exceso, forma diferentes tipos de estructuras, cada una con un nivel creciente de toxicidad para las neuronas:
- Monómeros: individualmente no son tóxicos, pero cuando se producen en grandes cantidades comienzan a unirse entre sí para formar estructuras dañinas. Es la primera señal de alarma de que el equilibrio se ha roto.
- Oligómeros: se forman cuando varios monómeros se unen creando pequeños grupos de 2 a 12 proteínas. Según algunos estudios, son los que causan la mayor toxicidad, afectando al 60% de las neuronas.
- Fibrillas y placas: son estructuras más grandes que se crean cuando los oligómeros continúan agregándose. Su presencia indica que el proceso degenerativo ya está muy avanzado.
Todos estos agregados tienen en común que alteran de manera progresiva las centrales energéticas de las neuronas, que se ven privadas del combustible para poderse comunicar y, en definitiva, funcionar de manera correcta.
Diagnóstico: cómo se detecta la acumulación de beta amiloide
Existen varias técnicas que permiten detectar la proteína amiloide:
Pruebas de imagen (PET cerebral)
La tomografía por emisión de positrones (PET) permite visualizar los depósitos de amiloide hasta 20 años antes de que aparezcan los síntomas evidentes de la enfermedad, así como otras alteraciones cerebrales y causas de deterioro cognitivo.
Para ello, se le administra al paciente por vía intravenosa una sustancia (conocida como trazador radiactivo) que se une selectivamente a las placas de beta amiloide.
Tras la administración, se espera entre 70 y 110 minutos para que el trazador se distribuya correctamente por el cerebro.
Esta técnica ofrece un diagnóstico con muy alta certeza en hasta el 40% de los pacientes.
Análisis del líquido cefalorraquídeo (LCR)
Es el complemento perfecto a la PET para ampliar o confirmar un diagnóstico, ya que la primera hace una fotografía visual de las placas en el cerebro, y el LCR informa sobre los niveles de diferentes proteínas:
- Beta-amiloide 1-42 (Aβ42): la forma perjudicial de la proteína.
- Beta-amiloide 1-40 (Aβ1-40): la forma deseada de la proteína.
- Ratio Aβ42/Aβ40: la proporción en la que están presenten ambas formas de la proteína, para distinguir con mayor precisión entre individuos con acumulación patológica de amiloide y aquellos sin ella.
- Proteína Tau: aunque no es específica de amiloide, la tau total y la tau fosforilada (pTau181) reflejan el daño neuronal y la formación de ovillos neurofibrilares, el segundo sello distintivo del alzhéimer junto a las placas amiloides.
Esta combinación tiene una elevada sensibilidad y especificidad diagnósticas para diferenciar la enfermedad de alzhéimer de otras demencias.
Estudios genéticos y biomarcadores asociados
Los estudios genéticos sirven para valorar el riesgo de desarrollar acumulación patológica de beta amiloide mediante el rastreo los principales genes implicados:
- APP (Proteína Precursora Amiloidea): localizado en el cromosoma 21, las mutaciones en este gen pueden aumentar la producción total de beta amiloide o favorecer las especies más patogénicas.
- PSEN1 y PSEN2 (Presenilinas 1 y 2): sus mutaciones se asocian con mayor producción de Aβ42 y una mayor relación Aβ42/Aβ40.
- ApoE: en especial, la variante ApoE4, que constituye el principal factor de riesgo genético para el alzhéimer esporádico y afecta al metabolismo de la beta amiloide.
Esta información se complementa con el análisis del biomarcador asociado más fiable, el de la proteína pTau217, con el que se podría detectar la patología amiloide mediante un simple análisis de sangre.
¿Es posible prevenir o reducir la beta amiloide?
Los avances en la investigación abren la puerta a la prevención de la beta amiloide, gracias a los fármacos existentes:
Fármacos dirigidos a la proteína beta amiloide
En 2024 tuvo lugar la aprobación de uno de los primeros fármacos capaces de modificar el curso de la enfermedad gracias a sus efectos sobre la beta amiloide.
Se trata del donanemab (Kisunla), un anticuerpo que reconoce la beta amiloide agregada en las placas cerebrales y facilita su eliminación.
Al eliminar estas placas tóxicas, el medicamento ayuda a restaurar la comunicación normal entre neuronas y reduce la inflamación cerebral crónica.
Los ensayos clínicos han mostrado que puede reducir la progresión del deterioro cognitivo en un 29% en comparación con placebo.
El segundo tratamiento, recientemente autorizado por la Comisión Europea en 2025, es el lecanemab (Leqembi).
Es otro anticuerpo que, en este caso, evita que las protofibrillas de beta-amiloide (las estructuras intermedias entre oligómeros y placas) formen placas maduras.
Sus resultados son prometedores: puede ralentizar la progresión del deterioro cognitivo en un 27% en personas con alzhéimer en etapas tempranas.
Además, se encuentra en desarrollo el trontinemab, que ha demostrado reducir la amiloide por debajo del umbral terapéutico en el 81% de los participantes.
Estilo de vida y factores de riesgo modificables
La influencia del estilo de vida está estudiada y confirmada: un estudio liderado por ISGlobal y el Barcelonaβeta Brain Research Center ha revelado que realizar ejercicio físico entre los 45 y 65 años puede reducir el riesgo de alzhéimer al disminuir la acumulación de beta amiloide.
Esto nos lleva a afirmar que ciertos cambios en los hábitos diarios pueden ser muy beneficiosos:
- Ejercicio físico: 150-300 minutos de actividad moderada por semana.
- Alimentación saludable: una dieta rica en frutas, verduras, cereales integrales, proteínas magras y grasas saludables (como las del pescado) se ha relacionado con niveles más bajos de placas y ovillos en los escáneres cerebrales.
- Sueño de calidad: el descanso favorece la eliminación de beta amiloide del cerebro y, lo contrario, la falta de sueño o el sueño de mala calidad pueden provocar una acumulación de esta proteína.
Además, mantener una actividad mental activa, tener conexiones sociales y la obtención de nuevos conocimientos son factores protectores que pueden retrasar el inicio de la enfermedad entre 5 y 7 años.
Investigación actual y tratamientos en desarrollo
A pesar de los logros en el tratamiento de la enfermedad de alzhéimer, la investigación sobre la beta amiloide continúa y arroja nuevos blancos y enfoques terapéuticos, como:
- Tratamientos dirigidos a los oligómeros tóxicos, en lugar de a las placas visibles. Se está estudiando la creación de péptidos sintéticos que los neutralizarían.
- Biomarcadores con mayor capacidad para controlar los niveles de beta amiloide, como la proteína LRP3.
- Ensayos clínicos en personas cognitivamente sanas con evidencia de acumulación de beta amiloide para estudiar la posible prevención del alzhéimer.
Este último experimento es especialmente relevante, porque va a permitir resolver la incógnita de si conviene intervenir antes de que aparezcan síntomas para prevenir completamente el desarrollo de la patología.
En definitiva: por primera vez en décadas tenemos herramientas para modificar el curso de la enfermedad.
Recuerda que nunca es demasiado tarde para hacer uso de ellas e implementar cambios saludables que puedan beneficiar la salud cerebral de la persona que cuidas.
Si tienes dudas, busca ayuda médica especializada y rodéate de otras personas que estén en tu misma situación para aprender estrategias.
En este sentido, desde Sanitas te recomendamos unirte a grupos de apoyo dirigidos por expertos, donde encontrarás información de calidad para resolver tus dudas y poder tomar mejores decisiones.
Consulta también nuestros consejos para afrontar el cuidado de una persona con alzhéimer, y aprende a cuidar bien. Nosotros también te acompañamos.